Физические и химические свойства алкенов. Химические свойства Физические и химические свойства алкенов таблица
ОПРЕДЕЛЕНИЕ
Алкены — непредельные углеводороды, молекулы которых содержат одну двойную связь; в названии алкенов присутствует суффикс –ен или -илен.
Общая формула гомологического ряда алкенов (табл. 2) – C n H 2n
Таблица 2. Гомологический ряд алкенов.
Углеводородные радикалы, образованные от алкенов: -CH = CH 2 – винил и –СН 2 -СН = СН 2 – аллил.
Для алкенов, начиная с бутена, характерна изомерия углеродного скелета:
СН 2 -С(СН 3)-СН 3 (2-метилпропен-1)
и положения двойной связи:
CH 2 = CH-CH 2 -CH 3 (бутен-1)
CH 3 -C = CH-CH 3 (бутен-2)
Для алкенов, начиная с бутена-2, характерна геометрическая (цис-транс) изомерия (рис. 1).
Рис. 1. Геометрические изомеры бутена-2.
Для алкенов, начиная с пропена, характерна межклассовая изомерия с циклоалканами. Так, составу C 4 H 8 отвечают вещества класса алкенов и циклоалканов – бутен-1(2) и циклобутан.
Атомы углерода в молекулах алкенов находятся в sp 2 -гибридизациии: 3σ-связи располагаются в одной плоскости под углом 120 друг к другу, а π-связь образована p-электронами соседних атомов углерода. Двойная связь является сочетанием σ- и π-связей.
Химические свойства алкенов
Большинство химических реакций алкенов протекают по механизму электрофильного присоединения:
— гидрогалогенирование – взаимодействие алкенов с галогенводородами (HCl, HBr), протекающее по правилу Марковникова (при присоединении полярных молекул типа НХ к несимметричным алкенам водород присоединяется к более гидрированному атому углерода при двойной связи)
CH 3 -CH = CH 2 + HCl = CH 3 -CHCl-CH 3
— гидратация — взаимодействие алкенов с водой в присутствии минеральных кислот (серной, фосфорной) с образованием спиртов, протекающее по правилу Марковникова
CH 3 -C(CH 3) = CH 2 + H 2 O = CH 3 -C(CH 3)OH-CH 3
— галогенирование — взаимодействие алкенов с галогенами, например, с бромом, при котором происходит обесцвечивание бромной воды
CH 2 = CH 2 + Br 2 = BrCH 2 -CH 2 Br
При нагревании смеси алкена с галогеном до 500С возможно замещение атома водорода алкена по радикальному механизму:
CH 3 -CH = CH 2 + Cl 2 = Cl-CH 2 -CH = CH 2 + HCl
По радикальному механизму протекает реакция гидрирования алкенов. Условием протекания реакции является наличие катализаторов (Ni, Pd, Pt), а также нагревание реакционной смеси:
CH 2 = CH 2 + H 2 = CH 3 -CH 3
Алкены способны окисляться с образованием различных продуктов, состав которых зависит от условий проведения реакции окисления. Так, при окислении в мягких условиях (окислитель – перманганат калия) происходит разрыв π-связи и образование двухатомных спиртов:
3CH 2 = CH 2 + 2KMnO 4 +4H 2 O = 3CH 2 (OH)-CH 2 (OH) +2MnO 2 + 2KOH
При жестком окислении алкенов кипящим раствором перманганата калия в кислой среде происходит полный разрыв связи (σ-связи) с образованием кетоны, карбоновых кислот или углекислого газа:
Окисление этилена кислородом при 200С в присутствии CuCl 2 и PdCl 2 приводит к образованию ацетальдегида:
CH 2 = CH 2 +1/2O 2 = CH 3 -CH = O
Алкены вступают в реакции полимеризации. Полимеризация — процесс образования высокомолекулярного соединения – полимера-путем соединения друг с другом с помощью главных валентностей молекул исходного низкомолекулярного вещества – мономера. Полимеризация может быть вызвана нагреванием, сверхвысоким давлением, облучением, действием свободных радикалов или катализаторов. Так, полимеризация этилена происходит под действием кислот (катионный механизм) или радикалов (радикальный механизм):
n CH 2 = CH 2 = -(-CH 2 -CH 2 -) n —
Физические свойства алкенов
При обычных условиях С 2 -С 4 – газы, С 5 -С 17 – жидкости, начиная с С 18 – твердые вещества. Алкены не растворимы в воде, хорошо растворимы в органических растворителях.
Получение алкенов
Основные способы получения алкенов:
— дегидрогалогенирование галогенпроизводных алканов под действием спиртовых растворов щелочей
CH 3 -CH 2 -CHBr-CH 3 + KOH = CH 3 -CH = CH-CH 3 + KBr + H 2 O
— дегалогенирование дигалогенпроизводных алканов под действием активных металлов
CH 3 -CHCl-CHCl-CH 3 + Zn = ZnCl 2 + CH 3 -CH = CH-CH 3
— дегидратация спиртов при их нагревании с серной кислотой (t >150 C) или пропускании паров спирта над катализатором
CH 3 -CH(OH)- CH 3 = CH 3 -CH = CH 2 + H 2 O
— дегидрирование алканов при нагревании (500С) в присутствии катализатора (Ni, Pt, Pd)
CH 3 -CH 2 — CH 3 = CH 3 -CH = CH 2 + H 2
Алкены применяются в качестве исходных продуктов в производстве полимерных материалов (пластмасс, каучуков, пленок) и других органических веществ.
Примеры решения задач
ПРИМЕР 1
| Задание | Установите молекулярную формулу алкена, если известно, что одно и тоже количество его, взаимодействуя с галогенами, образует, соответственно, или 56,5 г дихлорпроизводного или 101 г дибромпроизводного. |
| Решение |
Химические свойства алкенов определяются их способностью присоединять вещества по механизму электрофильного присоединения, при этом двойная связь превращается в одинарную:
СnH 2 n + Cl 2 → CnH 2 nCl 2 CnH 2 n + Br 2 → CnH 2 nBr 2 Масса алкена, вступившего в реакцию одна и та же, значит в реакции участвует одинаковое количество моль алкена. Выразим количество моль углеводорода, если молярная масса дихлорпроизводного 12n+2n+71, молярная масса дибромпроизводного (12n+2n+160): m(CnH 2 nCl 2) \ (12n+2n+71) = m(СnH 2 nBr 2) \ (12n+2n+160) 56.5 \ (12n+2n+71) = 101 \ (12n+2n+160) Следовательно, алкен имеет формулу C 3 H 6 – это пропен. |
| Ответ | Формула алкена C 3 H 6 – это пропен |
ПРИМЕР 2
| Задание | Осуществите ряд превращений этан → этен → этанол → этен → хлорэтан → бутан |
| Решение |
Для получения этена из этана необходимо использовать реакцию дегидрирования этана, которая протекает в присутствии катализатора (Ni, Pd, Pt) и при нагревании:
С 2 H 6 →C 2 H 4 + H 2 Получение этанола из этена осуществляют по реакции гидратации, протекающей водой в присутствии минеральных кислот (серной, фосфорной): С 2 H 4 + H 2 O = C 2 H 5 OH Для получения этена из этанола используют реакцию дегидротации: C 2 H 5 OH →(t, H 2 SO 4) → C 2 H 4 + H 2 O Получение хлорэтана из этена осуществляют по реакции гидрогалогенирования: С 2 H 4 + HCl → C 2 H 5 Cl Для получения бутана из хлорэтана используют реакцию Вюрца: 2C 2 H 5 Cl +2Na → C 4 H 10 + 2NaCl |
Содержащие пи-связь - это непредельные углеводороды. Они являются производными алканов, в молекулах которых произошло отщепление двух атомов водорода. Образовавшиеся свободные валентности формируют новый тип связи, которая располагается перпендикулярно плоскости молекулы. Так возникает новая группа соединений - алкены. Физические свойства, получение и применение веществ этого класса в быту и промышленности мы рассмотрим в этой статье.
Гомологический ряд этилена
Общая формула всех соединений, называемых алкенами, отражающая их качественный и количественный состав, - это C n H 2 n . Названия углеводородов по систематической номенклатуре имеют следующий вид: в термине соответствующего алкана изменяется суффикс с -ан на -ен, например: этан - этен, пропан - пропен и т. д. В некоторых источниках можно встретить еще одно название соединений этого класса - олефины. Далее мы изучим процесс образования двойной связи и физические свойства алкенов, а также определим их зависимость от строения молекулы.
Как образуется двойная связь
Электронную природу пи-связи на примере этилена можно представить следующим образом: атомы карбона в его молекуле находятся в форме sp 2 -гибридизации. В этом случае формируется сигма-связь. Еще две гибридные орбитали - по одной от атомов углерода, формируют простые сигма-связи с водородными атомами. Два оставшихся свободных гибридных облака атомов карбона перекрываются над и под плоскостью молекулы - образуется пи-связь. Именно она определяет физические и химические свойства алкенов, речь о которых пойдет далее.

Пространственная изомерия
Соединения, имеющие один и тот же количественный и качественный состав молекул, но различное пространственное строение, называются изомерами. Изомерия встречается в группе веществ, называемых органическими. На характеристику олефинов большое влияние оказывает явление оптической изомерии. Она выражается в том, что гомологи этилена, содержащие у каждого из двух углеродных атомов при двойной связи различные радикалы или заместители, могут встречаться в форме двух оптических изомеров. Они отличаются друг от друга положением заместителей в пространстве относительно плоскости двойной связи. Физические свойства алкенов в этом случае также будут разными. Например, это касается температур кипения и плавления веществ. Так, олефины неразветвленного строения углеродного скелета имеют более высокие температуры кипения, чем соединения-изомеры. Также температуры кипения цис-изомеров алкенов выше, чем транс-изомеров. В отношении температур плавления картина противоположная.
Сравнительная характеристика физических свойств этилена и его гомологов
Первые три представителя олефинов являются газообразными соединениями, затем, начиная с пентена C 5 H 10 и до алкена с формулой C 17 H 34 , - жидкости, а далее идут твердые вещества. У гомологов этена прослеживается следующая тенденция: температуры кипения соединений снижаются. Например, у этилена этот показатель равен -169,1°C, а у пропилена -187,6°C. Зато температуры кипения с увеличением молекулярной массы повышаются. Так, у этилена она равна -103,7°C, а у пропена -47,7°C. Подводя итог сказанному, можно сделать вывод, звучащий кратко: физические свойства алкенов зависят от их молекулярной массы. С ее увеличением изменяется агрегатное состояние соединений в направлении: газ - жидкость - твердое вещество, а также снижается температура плавления, а температуры кипения возрастают.

Характеристика этена
Первый представитель гомологического ряда алкенов - это этилен. Он является газом, малорастворимым в воде, но хорошо растворяющимся в органических растворителях, не имеющим цвета. Молекулярная масса - 28, этен немного легче воздуха, имеет едва уловимый сладковатый запах. Он легко вступает в реакции с галогенами, водородом и галогеноводородами. Физические свойства алкенов и парафинов тем не менее достаточно близки. Например, агрегатное состояние, способность метана и этилена к жесткому окислению и т. д. Как же можно различить алкены? Как выявить непредельный характер олефина? Для этого существуют качественные реакции, на которых мы и остановимся подробнее. Напомним, какую особенность в строении молекулы имеют алкены. Физические и химические свойства этих веществ определяются наличием в их составе двойной связи. Чтобы доказать ее присутствие, пропускают газообразный углеводород через фиолетовый раствор перманганата калия или бромную воду. Если они обесцветились, значит, соединение содержит в составе молекул пи-связи. Этилен вступает в реакцию окисления и обесцвечивает растворы KMnO 4 и Br 2 .
Механизм реакций присоединения
Разрыв двойной связи заканчивается присоединением к свободным валентностям карбона атомов других химических элементов. Например, при взаимодействии этилена с водородом, называемом гидрогенизацией, получается этан. Необходим катализатор, например порошковидный никель, палладий или платина. Реакция с HCl заканчивается образованием хлорэтана. Алкены, содержащие более двух атомов углерода в составе своих молекул, проходят реакцию присоединения галогеноводородов с учетом правила В. Марковникова.

Как гомологи этена взаимодействуют с галогеноводородами
Если перед нами стоит задание "Охарактеризуйте физические свойства алкенов и их получение", нам нужно рассмотреть правило В. Марковникова более подробно. Практическим путем установлено, что гомологи этилена реагируют с хлороводородом и другими соединениями по месту разрыва двойной связи, подчиняясь некоторой закономерности. Она заключается в том, что атом водорода присоединяется к наиболее гидрогенизированному углеродному атому, а ион хлора, брома или йода - к карбоновому атому, содержащему наименьшее количество атомов водорода. Эта особенность протекания реакций присоединения получила название правила В. Марковникова.
Гидратация и полимеризация
Продолжим далее рассматривать физические свойства и применение алкенов на примере первого представителя гомологического ряда - этена. Его реакция взаимодействия с водой используется в промышленности органического синтеза и имеет важное практическое значение. Впервые процесс был проведен еще в XIX веке А.М. Бутлеровым. Реакция требует выполнения ряда условий. Это, прежде всего, использование концентрированной серной кислоты или олеума в качестве катализатора и растворителя этена, давление порядка 10 атм и температура в пределах 70°. Процесс гидратации происходит в две фазы. Вначале по месту разрыва пи-связи к этену присоединяются молекулы сульфатной кислоты, при этом образуется этилсерная кислота. Затем полученное вещество реагирует с водой, получается этиловый спирт. Этанол - важный продукт, применяемый в пищевой промышленности для получения пластмасс, синтетических каучуков, лаков и других продуктов органической химии.

Полимеры на основе олефинов
Продолжая изучать вопрос применения веществ, относящихся к классу алкенов, изучим процесс их полимеризации, в котором могут участвовать соединения, содержащие непредельные химические связи в составе своих молекул. Известно несколько типов реакции полимеризации, по которым происходит образование высокомолекулярных продуктов - полимеров, например таких как полиэтилен, полипропилен, полистирол и т. д. Свободнорадикальный механизм приводит к получению полиэтилена высокого давления. Это одно из наиболее широко применяемых соединений в промышленности. Катионно-ионный тип обеспечивает получение полимера стереорегулярного строения, например полистирола. Он считается одним из наиболее безопасных и удобных в использовании полимеров. Изделия из полистирола устойчивы к агрессивным веществам: кислотам и щелочам, негорючие, легко окрашиваются. Еще один вид механизма полимеризации - димеризация, он приводит к получению изобутена, применяемого в качестве антидетонационной добавки к бензину.
Способы получения
Алкены, физические свойства которых мы изучаем, получают в лабораторных условиях и промышленности различными методами. В опытах в школьном курсе органической химии используют процесс дегидратации этилового спирта с помощью водоотнимающих средств, например таких, как пятиокись фосфора или сульфатная кислота. Реакция проводится при нагревании и является обратной процессу получения этанола. Еще один распространенный способ получения алкенов нашел свое применение в промышленности, а именно: нагревание галогенопроизводных предельных углеводородов, например хлорпропана с концентрированными спиртовыми растворами щелочей - гидроксида натрия или калия. В реакции происходит отщепление молекулы хлороводорода, по месту появления свободных валентностей атомов карбона образуется двойная связь. Конечным продуктом химического процесса будет олефин - пропен. Продолжая рассматривать физические свойства алкенов, остановимся на главном процессе получения олефинов - пиролизе.

Промышленное производство непредельных углеводородов ряда этилена
Дешевое сырье - газы, образующиеся в процессе крекинга нефти, служат источником получения олефинов в химической промышленности. Для этого применяют технологическую схему пиролиза - расщепление газовой смеси, идущее с разрывом углеродных связей и образованием этилена, пропена и других алкенов. Пиролиз проводят в специальных печах, состоящих из отдельных пирозмеевиков. В них создается температура порядка 750-1150°C и присутствует водяной пар в качестве разбавителя. Реакции происходят по цепному механизму, идущему с образованием промежуточных радикалов. Конечный продукт - это этилен или пропен, их получают в больших объемах.

Мы подробно изучили физические свойства, а также применение и способы получения алкенов.
Физические свойства алкенов похожи на свойства алканов, хотя все они имеют несколько более низкие температуры плавления и кипения, чем соответствующие алканы. Например, пентан имеет температуру кипения 36 °С, а пентен-1 - 30 °С. При обычных условиях алкены С 2 — С 4 - газы. С 5 – С 15 - жидкости, начиная с C 16 - твердые вещества. Алкены не растворимы в воде, хорошо растворимы в органических растворителях.
В природе алкены встречаются редко. Поскольку алкены являются ценным сырьем для промышленного органического синтеза, разработаны многие способы их получения.
1. Основным промышленным источником алкенов служит крекинг алканов, входящих в состав нефти:
3. В лабораторных условиях алкены получают по реакциям отщепления (элиминирования), при которых от соседних атомов углерода отщепляются два атома или две группы атомов, и образуется дополнительная p -связь. К таким реакциям относятся следующие.
1) Дегидратация спиртов происходит при их нагревании с водоотнимающими средствами, например с серной кислотой при температуре выше 150 °С:
При отщеплении Н 2 O от спиртов, НВr и HCl от алкилгалогенидов атом водорода преимущественно отщепляется от того из соседних атомов углерода, который связан с наименьшим числом атомов водорода (от наименее гидрогенизированного атома углерода). Эта закономерность носит название правила Зайцева .
3) Дегалогенирование происходит при нагревании дигалогенидов, имеющих атомы галогена у соседних атомов углерода, с активными металлами:
CH 2 Br —CHBr —CH 3 + Mg → СН 2 =СН-СН 3 + Mg Вr 2 .
Химические свойства алкенов определяются наличием в их молекулах двойной связи. Электронная плотность p -связи достаточно подвижна и легко вступает в реакции с электрофильными частицами. Поэтому многие реакции алкенов протекают по механизму электрофильного присоединения , обозначаемому символом A E (от англ, addition electrophilic ). Реакции злектрофильного присоединения это ионные процессы, протекающие в несколько стадий.
На первой стадии электрофильная частица (чаще всего это бывает протон H +) взаимодействует с p -электронами двойной связи и образует p -комплекс, который затем превращается в карбокатион путем образования ковалентной s -связи между электрофильной частицей и одним из атомов углерода:
алкен p -комплекс карбокатион
На второй стадии карбокатион реагирует с анионом X — , образуя вторую s -связь за счет электронной пары аниона:
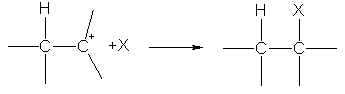
Ион водорода в реакциях электрофильного присоединения присоединяется к тому из атомов углерода при двойной связи, на котором больше отрицательный заряд. Распределение зарядов определяется смещением p
-электронной плотности под влиянием заместителей:  .
.
Электронодонорные заместители, проявляющие +I -эффект, смещают p -электронную плотность к более гидрогенизированному атому углерода и создают на нем частичный отрицательный заряд. Этим объясняется правило Марковникова : при присоединении полярных молекул типа НХ(X = Hal , ОН, CN и т.п.) к несимметричным алкенам водород преимущественно присоединяется к более гидрогенизированному атому углерода при двойной связи.
Рассмотрим конкретные примеры реакций присоединения.
1) Гидрогалогенирование . При взаимодействии алкенов с галогеноводородами (HCl , НВr ) образуются алкилгалогениды:
СН 3 -СН=СН 2 + НВr ® СН 3 -СНВr-СН 3 .
Продукты реакции определяются правилом Марковникова.
Следует, однако, подчеркнуть, что в присутствии какого-либо органического пероксида полярные молекулы НХ реагируют с алкенами не по правилу Марковникова:
| R-O-O-R | ||
| СН 3 -СН=СН 2 + НВr | СН 3 -СН 2 -СН 2 Вr |
Это связано с тем, что присутствие перекиси обусловливает радикальный, а не ионный механизм реакции.
2) Гидратация . При взаимодействии алкенов с водой в присутствии минеральных кислот (серной, фосфорной) образуются спирты. Минеральные кислоты выполняют роль катализаторов и являются источниками протонов. Присоединение воды также идет по правилу Марковникова:
СН 3 -СН=СН 2 + НОН ® СН 3 -СН(ОН)-СН 3 .
3) Галогенирование . Алкены обесцвечивают бромную воду:
СН 2 =СН 2 + Вr 2 ® ВrСН 2 -СН 2 Вr.
Эта реакция является качественной на двойную связь.
4) Гидрирование . Присоединение водорода происходит под действием металлических катализаторов:
где R = Н, СН 3 , Cl , С 6 Н 5 и т.д. Молекула CH 2 =CHR называется мономером, полученное соединение - полимером , число n-степень полимеризации.
Полимеризация различных производных алкенов дает ценные промышленные продукты: полиэтилен, полипропилен, поливинилхлорид и другие.
Кроме присоединения, для алкенов характерны также реакции окисления. При мягком окислении алкенов водным раствором перманганата калия (реакция Вагнера ) образуются двухатомные спирты:
ЗСН 2 =СН 2 + 2КМn О 4 + 4Н 2 О ® ЗНОСН 2 -СН 2 ОН + 2MnO 2 ↓ + 2KOH .
В результате протекания этой реакции фиолетовый раствор перманганата калия быстро обесцвечивается и выпадает коричневый осадок оксида марганца (IV ). Эта реакция, как и реакция обесцвечивания бромной воды, является качественной на двойную связь. При жестком окислении алкенов кипящим раствором перманганата калия в кислой среде происходит полный разрыв двойной связи с образованием кетонов, карбоновых кислот или СО 2 , например:
| [О] | ||
| СН 3 -СН=СН-СН 3 | 2СН 3 -СООН |
По продуктам окисления можно установить положение двойной связи в исходном алкене.
Как и все другие углеводороды, алкены горят, и при обильном доступе воздуха образуют диоксид углерода и воду:
С n Н 2 n + Зn /2О 2 ® n СО 2 + n Н 2 О.
При ограниченном доступе воздуха горение алкенов может приводить к образованию монооксида углерода и воды:
С n Н 2n + nО 2 ® nCO + nH 2 O .
Если смешать алкен с кислородом и пропустить эту смесь над нагретым до 200°С серебряным катализатором, то образуется оксид алкена (эпоксиалкан), например:

При любых температурах алкены окисляются озоном (озон более сильный окислитель, чем кислород). Если газообразный озон пропускают через раствор какого-либо алкена в тетрахлор-метане при температурах ниже комнатной, то происходит реакция присоединения, и образуются соответствующие озониды (циклические перекиси). Озониды очень неустойчивы и могут легко взрываться. Поэтому обычно их не выделяют, а сразу после получения разлагают водой - при этом образуются карбонильные соединения (альдегиды или кетоны), строение которых указывает на строение подвергавшегося озонированию алкена.
Низшие алкены - важные исходные вещества для промышленного органического синтеза. Из этилена получают этиловый спирт, полиэтилен, полистирол. Пропен используют для синтеза полипропилена, фенола, ацетона, глицерина.
Алкены — это непредельные углеводороды , которые имеют одну двойную связь между атомами . Другое их название это олефины, оно связано с историей открытия этого класса соединений. В основном в природе эти вещества не встречаются, а синтезируются человеком для практических целей. В номенклатуре ИЮПАК название этих соединений формируется по тому же принципу, что и для алканов, только суффикс “ан” заменяется на “ен”.
Вконтакте
Строение алкенов
Два атома углерода, участвующих в образовании двойной связи, всегда находятся в sp2 гибридизации, и угол между ними равен 120 градусам. Двойная связь образована с помощью перекрывания π -π орбиталей, а оно не очень прочное, поэтому данную связь достаточно просто разорвать, что находит применение в химических свойствах веществ.
Изомерия
По сравнению с предельными, в этих углеводородах возможно больше видов , при том как пространственной, так и структурной. Структурная изомерия может также подразделяться на несколько видов.
Первый также существует и для алканов, и заключается в различном порядке соединения атомов углерода. Так изомерами могут быть пентен-2 и 2-метилбутен-2. А второй — это изменение положения двойной связи.
Пространственная изомерия в этих соединениях возможна благодаря появлению двойной связи. Она бывает двух видов — геометрической и оптической.
Геометрическая изомерия — один из самых распространенных в природе видов, при том практически всегда геометрические изомеры будут иметь кардинально разные физические и химические свойства. Различают цис и транс изомеры. У первых — заместители располагаются с одной стороны от кратной связи, а у транс изомеров они находятся в разных плоскостях.
Получение алкенов
 Впервые получены они были, как и много других веществ, совершенно случайно.
Впервые получены они были, как и много других веществ, совершенно случайно.
Немецкий химик и исследователь Бехер в конце 17 века изучал действие серной кислоты на этиловый спирт и понял, что получил неизвестный газ , который при этом является более реакционноспособным, чем метан.
Позже подобные исследования провели еще несколько ученых, они же и узнали, что данный газ при взаимодействии с хлором образует маслянистое вещество.
Поэтому первоначально этому классу соединений было присвоено название олефины, что переводится как маслородный. Но все же определить состав и строение данного соединения у ученых не получалось. Это произошло только почти спустя два века, в конце девятнадцатого столетия.
В настоящее время существует много способов получения алкенов.
Промышленные способы
Получение промышленными методами :
- Дегидрирование предельных углеводородов. Данная реакция возможна только при действии высоких температур (около 400 градусов) и катализаторов — либо оксида хрома 3, либо алюмоплатиновых катализаторов.
- Дегалогенирование дигалогеноалканов. Происходит только в присутствии цинка или магния, и при высоких температурах.
- Дегидрогалогенирование галогеноалканов. Проводится при помощи натриевых или калиевых солей органических кислот при повышенной температуре.
Важно ! Данные способы получения алкенов не дают чистого продукта, результатом реакции будет смесь непредельных углеводородов. Преобладающее среди них соединение определяется с помощью правила Зайцева. Оно гласит, что водород отщепляется с наибольшей вероятностью от атома углерода у которого меньше всего связей с водородами.
Дегидратация спиртов. Может проводиться только при нагревании и в присутствии растворов сильных минеральных кислот, обладающих водоотнимающим свойством.
Гидрирование алкинов. Возможно только в присутствии паладиевых катализаторов.
Химические свойства алкенов
Алкены являются очень химически активными веществами. Во многом это объясняется благодаря наличию двойной связи. Самыми характерными реакциями для этого класса соединений являются электрофильное и радикальное присоединение.
- Галогенирование алкенов — относится к классическим реакциям электрофильного присоединения. Она происходит только в присутствии инертных органических растворителей, чаще всего это тетрахлорметан.
- Гидрогалогенирование. Присоединение этого типа осуществляется по правилу Марковникова. Ион присоединяется к более гидрированному атому углерода возле двойной связи, и соответственно, ион галогенида присоединяется ко второму атому углерода. Это правило нарушается в присутствии перекисных соединений — эффект Харроша. Присоединение галогеноводорода происходит полностью обратно правилу Марковникова.
- Гидроборирование. Эта реакция имеет значительную практическую важность. Поэтому ученый, который ее открыл и изучил даже получил Нобелевскую премию. Данная реакция проводится в несколько ступеней, при этом присоединение иона бора происходит не по правилу Марковникова.
- Гидратация алкенов или присоединение . Данная реакция также протекает согласно правилу Марковникова. Гидроксид-ион присоединяется к наименее гидрированному атому углерода при двойной связи.
- Алкилирование — еще одна реакция часто применяемая в промышленности. Она заключается в присоединении предельных углеводородов к непредельным под воздействием низких температур и катализаторов, с целью увеличения атомной массы соединений. Катализатором чаще всего выступают сильные минеральные кислоты. Также эта реакция может протекать и по свободнорадикальному механизму.
- Полимеризация алкенов — еще одна нехарактерная для предельных углеводородов реакция. Она подразумевает соединение между собой многочисленных молекул с целью образования прочного соединения, отличающегося по своим физическим свойствам.
 n в данной реакции это количество молекул, вступивших в связь. Обязательным условием осуществления является кислая среда, повышенная температура и увеличенное давление.
n в данной реакции это количество молекул, вступивших в связь. Обязательным условием осуществления является кислая среда, повышенная температура и увеличенное давление.
Также для алкенов характерны и другие реакции электрофильного присоединения, которые не получили такого обширного практического распространения.
Например, реакция присоединения спиртов, с образованием простых эфиров.
Или присоединение хлорангидридов, с получением непредельных кетонов — реакция Кондакова.
Обратите внимание! Данная реакция возможна только в присутствии катализатора хлорида цинка.
Следующий крупный класс реакций характерный для алкенов это реакции радикального присоединения. Данные реакции возможны только при образовании свободных радикалов под воздействием высоких температур, облучения и других действий. Самая характерная реакция радикального присоединения это гидрирование с образованием предельных углеводородов. Она происходит исключительно под воздействием температур и в присутствии платинового катализатора.
Благодаря наличию двойной связи, для алкенов очень характерными являются различные реакции окисления .
- Горение — классическая реакция окисления. Она хорошо идет без катализаторов. В зависимости от количества кислорода возможны разные конечные продукты: от углекислого газа и до углерода.
- Окисление перманганатом калия в нейтральной среде. Продуктами являются многоатомные спирты и бурый осадок диоксида марганца. Данная реакция считается качественной для алкенов.
- Также мягкое окисление может осуществляться пероксидом водорода, оксидом осмия 8, и другими окислителями в нейтральной среде. Для мягкого окисления алкенов характерен разрыв только одной связи, продуктом реакции, как правило, являются многоатомные спирты.
- Также возможно и жесткое окисление, при котором происходит разрыв обеих связей и образуются кислоты или кетоны. Обязательным условием является кислая среда, чаще всего используют серную кислоту, так как другие кислоты могут также подвергаться окислению с образованием побочных продуктов.
Физические свойства алкенов
 Газами в нормальных условиях являются только этилен, пропен и бутен.
Газами в нормальных условиях являются только этилен, пропен и бутен.
Начиная с пентена, и до гептодецена, все алкены находятся в жидком состоянии.
И все остальные являются твердыми веществами.
Температуры плавления и кипения пропорционально увеличиваются с ростом молекулярной массы, но могут меняться для изомеров.
Все алкены не растворяются в воде , но хорошо растворяются в инертных органических растворителях.
Применение алкенов
Алкены довольно широко используются в промышленности и применяются для синтеза большого количества веществ. Например, при помощи этилена синтезируют поливинилхлорид(ПВХ), стирол, этиленгликоль, этанол, полиэтилен, каучуки и множество других веществ. Наибольший объем пропилена используют для получения полипропилена.
Алкены — строение, свойства, применение
Изучаем химию — свойства алкенов, применение в промышленности
Вывод
В общем, можно точно сказать, что алкены благодаря своим химическим свойствам являются очень востребованными в промышленности. Они участвуют в производстве самых разнообразных пластмасс, каучуков и множества других веществ.
Для алкенов характерны, прежде всего, реакции присоединения по двойной связи. В основном эти реакции идут по ионному механизму. Пи-связь разрывается, и образуются две новые сигма-связи. Напомню, что для алканов типичными были реакции замещения и шли они по радикальному механизму. Присоединяться к алкенам могут молекулы водорода, эти реакции называются гидрирование, молекулы воды, гидратация, галогены галогенирование, галогенводороды гидрогалогенирование. Но обо всем по порядку.
Реакции присоединения по двойной связи
Итак, первое химическое свойство способность присоединять галогеноводороды, гидрогалогенирование.
Пропен и остальные алкены реагируют с галогеноводородами по правилу Марковникова.

Атом водорода присоединяется к наиболее гидрированному, или правильнее сказать гидрогенизированному, атому углерода.
Вторым номером в нашем списке свойств будет гидратация, присоединение воды.
Реакция проходит при нагревании в присутствии кислоты обычно серной или фосфорной. Присоединение воды происходит также по правилу Марковникова, то есть первичный спирт можно получить только гидратацией этилена, остальные неразветвленные алкены дают вторичные спирты.

И для гидрогалогениерования и для гидратации существуют исключения из правила Марковникова. Во-первых, против этого правила присоединение протекает в присутствии пероксидов.
Во-вторых, для производных алкенов, в которых присуствуют электронноакцепторне группы. Например, для 3,3,3-трифторпропена-1.

Атомы фтора за счет высокой электроотрицательности оттягивают на себя электронную плотность по цепи сигма-связей. Такое явление называется отрицательным индуктивным эффектом.

Из-за этого происходит смещение подвижных пи-электронов двойной связи и у крайнего атома углерода оказывается частичный положительный заряд, который обычно обозначается как дельта плюс. Именно к нему и пойдет отрицательно заряженный ион брома, а катион водорода присоединится к наименее гидрированному атому углерода.
Помимо трифторметильной группы отрицательным индуктивным эффектом обладает, например, трихлорметильная группа, нитрогруппа, карбоксильная группа и некоторые другие.
Этот второй случай нарушения правила Марковникова в ЕГЭ встречается очень редко, но все-таки желательно иметь его в виду, если вы планируете сдать экзамен на максимальный балл.
Третье химическое свойство присоединение молекул галогенов.
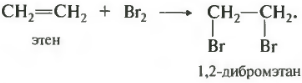
В первую очередь это касается брома, поскольку данная реакция является качественной на кратную связь. При пропускании, например, этилена через бромную воду, то есть раствор брома в воде, имеющий коричневый цвет, происходит ее обесцвечивание. Если пропускать через бромную воду смесь газов, например, этан и этен, то можно получить чистый этан без примеси этена, поскольку тот останется в реакционной колбе в виде дибромэтана, представляющего собой жидкость.
Особым образом стоит отметить реакцию алкенов в газовой фазе при сильном нагревании, например, с хлором.
При таких условиях протекает не реакция присоединения, а реакция замещения. При чем исключительно по альфа-атому углерода, то есть атому, соседствующему с двойной связью. В данном случае получается 3-хлорпропен-1. Эти реакции на экзамене встречаются нечасто, поэтому большинство учеников их не помнит и, как правило, совершает ошибки.
Четвертым номером идет реакция гидрирования, а вместе с ней и реакция дегидрирования. То есть присоединение или отщепление водорода.
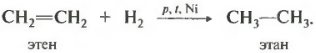
Гидрирование происходит при не очень высокой температуре на никелевом катализаторе. При более высокой температуре возможно дегидрирование с получением алкинов.
Пятым свойством алкенов является способность к полимеризации, когда сотни и тысячи молекул алкена за счет разрыва пи-связи и образования сигма-свзяей друг с другом образуют очень длинные и прочные цепочки.
В данном случае получился полиэтилен. Обратите внимание, что в получившейся молекуле кратные связи отсутствуют. Такие вещества называются полимерами, исходные молекулы называются мономерами, повторяющийся фрагмент это элементарное звено полимера, а число n степень полимеризации.
Также возможны реакции получения других важных полимерных материалов, например, полипропилена.


Еще один важный полимер поливинилхлорид.

Исходным веществом для производства этого полимера является хлорэтен, тривиальное название которого винилхлорид. Поскольку этот непредельный заместитель называется винил. Часто встречающаяся аббревиатура на пластмассовых изделиях ПВХ как раз расшифровывается как поливинилхлорид.
Мы обсудили пять свойств, которые представляли собой реакции присоединения по двойной связи. Теперь обратимся к реакциям окисления .
Реакции окисления алкенов
Шестое химическое свойство в нашем общем списке это мягкое окисление или реакция Вагнера. Оно протекает при воздействии на алкен водным раствором перманганата калия на холоду, поэтому часто в экзаменационных заданиях указывают температуру ноль градусов.
В результате получается двухатомный спирт. В данном случае этиленгликоль, а в целом такие спирты носят общее название гликоли. В процессе реакции фиолетово-розовый раствор перманганата обесцвечивается, поэтому эта реакция также является качественной на двойную связь. Марганец в нейтральной среде из степени окисления +7 восстанавливается до степени окисления +4. Рассмотрим еще несколько примеров. УРАВНЕНИЕ
Здесь получился пропандиол-1,2. Однако таким же образом будут реагировать и циклические алкены. УРАВНЕНИЕ
Еще один вариант, когда двойная связь находится, например, в боковой цепи ароматических углеводородов. Регулярно в заданиях егэ встречается реакция Вагнера с участием стирола, его второе название винилбензол.

Я надеюсь, что представил вашему вниманию достаточно примеров, чтобы вы поняли, что мягкое окисление двойной связи всегда подчиняется довольно простому правилу пи-связь разрывается и к каждому атому углерода присоединяется гидроксигруппа.
Теперь, что касается жесткого окисления. Это будет наше седьмое свойство. Такое окисление происходит, когда алкен реагирует с кислотным раствором перманганата калия при нагревании.
Происходит деструкция молекулы, то есть ее разрушение по двойной связи. В случае бутена-2 получились две молекулы уксусной кислоты. В целом же, по продуктам окисления можно судить о положении кратной связи в углеродной цепи.
При окислении бутена-1 получается молекула пропионовой (пропановой) кислоты и углекислый газ.
В случае этилена получится две молекулы углекислого газа. Во всех случаях в кислой среде марганец из степени окисления +7 восстанавливается до +2.
И, наконец, восьмое свойство полное окисление или горение.
Алкены сгорают, как и другие углеводороды, до углекислого газа и воды. Запишем уравнение сгорания алкенов в общем виде.
Молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле алкена, поскольку в состав молекулы CO 2 входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть 2n/2, а значит просто n.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа плюс n из воды, итого 3n. Слева атомов кислорода столько же, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть 3n/2 молекул кислорода. Можно записать 1,5n.
Мы рассмотрели восемь химических свойств алкенов.
Возможно, будет полезно почитать:
- Себестоимость продукции на предприятии ;
- Каковы причины мужского бесплодия? ;
- Препараты, которые вызывают галлюцинации ;
- Презентация на тему иван калита Дань для Золотой Орды ;
- Когда ставить памятник после похорон? ;
- Рецепт приготовления вкусной гречки на гарнир Гречка гарнир что добавить для пикантности ;
- Печенье «Олимпийский мишка ;
- Курица, маринованная в кефире ;